





来源:医疗器械创新网|
发表时间:2019-01-07
点击:12538
文章来源:医疗器械经销商联盟、国家药品监督管理局
12月10日,国家药监局综合司发布《关于2019年医疗器械行业标准制修订计划项目公示》。
按照《医疗器械标准管理办法》《医疗器械标准制修订工作管理规范》要求,国家药品监督管理局组织开展了2019年医疗器械行业标准制修订项目遴选工作,经公开征求意见和组织专家论证,确定了2019年94项医疗器械行业标准制修订计划项目,现予以公示。
其中包括医用电气设备、体外诊断设备及试剂、骨科相关设备等94项医疗器械行业标准制修订计划,包括新制定和修订。
随着新标准的修订、制订,原来没有的标准将被制订,原来已有的部分标准,将除旧立新。
标准,缘于市场或既有的产品,企业参与起草也十分常见,从一些大公司的简介中都能看到“参考了xx项行业标准制订”等字样。
而标准之争,也将是企业界最高级别的竞争形态,它可能不是紧急的,但一定是非常重要的。
谁掌握了标准,谁就更有竞争力。所以,不要小看行业标准的制订、修订,你终会发现它的力量不知道在哪一天爆发出来。
|
按照《医疗器械标准管理办法》《医疗器械标准制修订工作管理规范》要求,国家药品监督管理局组织开展了2019年医疗器械行业标准制修订项目遴选工作,经公开征求意见和组织专家论证,确定了2019年94项医疗器械行业标准制修订计划项目,现予以公示。公示期间,如对计划项目有异议,请向国家药品监督管理局反馈。
公示时间:2018年12月11日至12月17日
联系人及电话:黄伦亮,010-88331421
通讯地址:北京市西城区宣武门西大街26号院2号楼国家药品监督管理局器械注册司
邮编:100053
国家药监局综合司 2018年12月10日 |
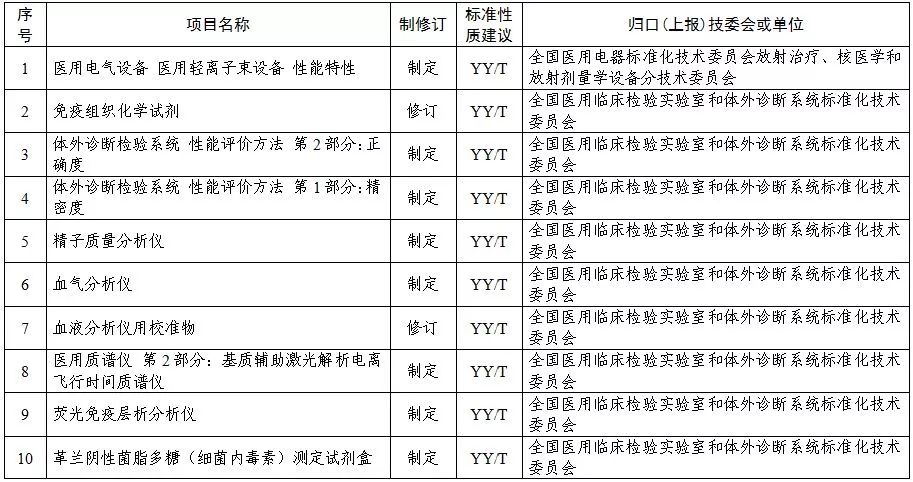
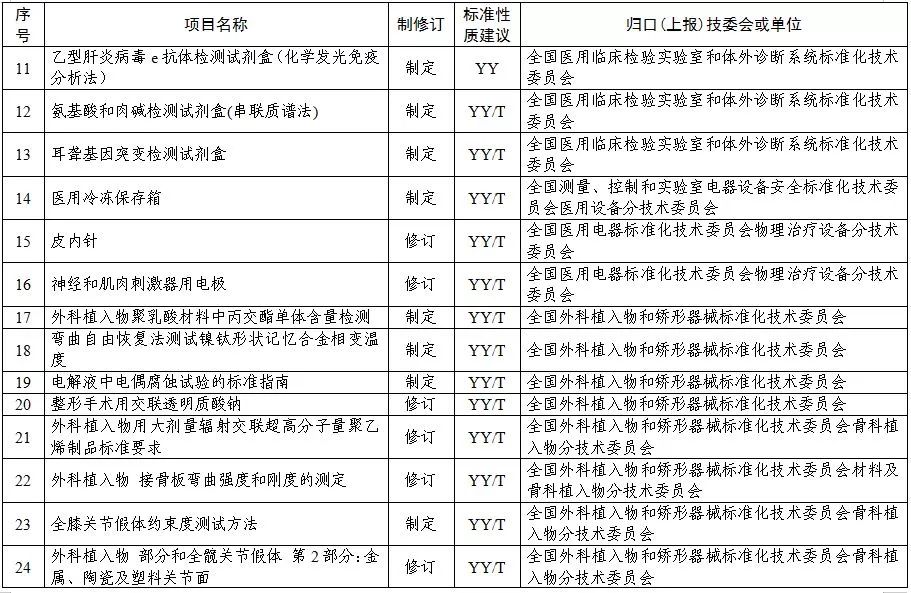
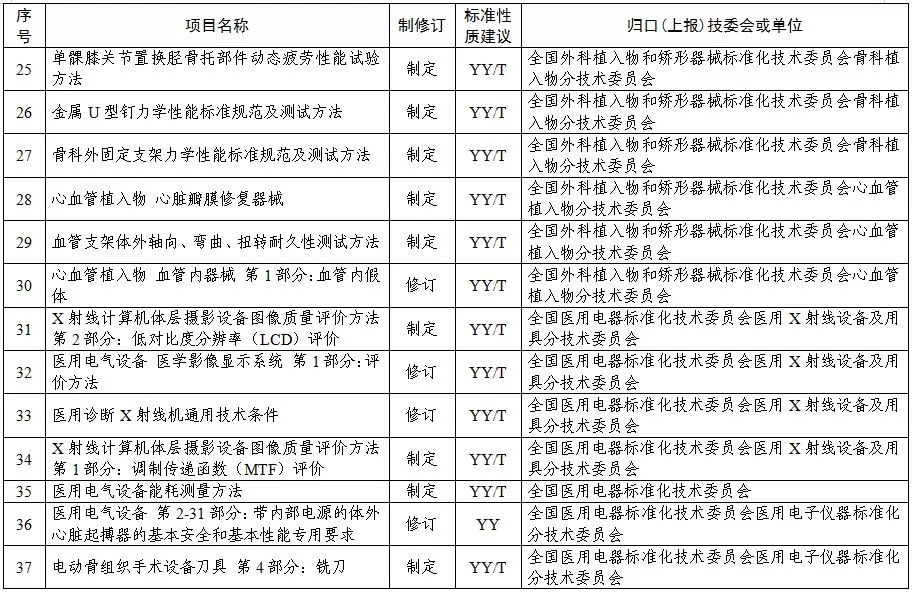
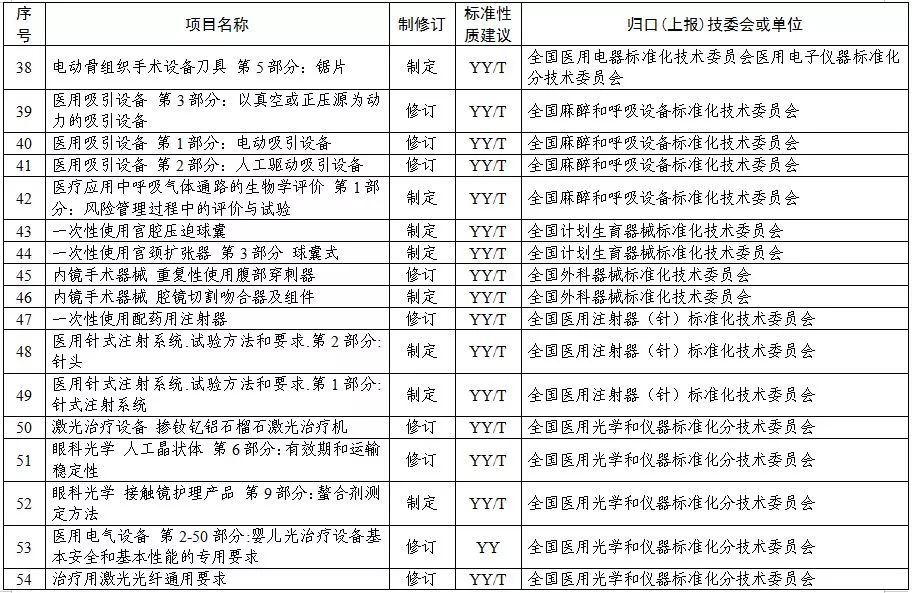
2019年医疗器械行业标准制修订计划项目
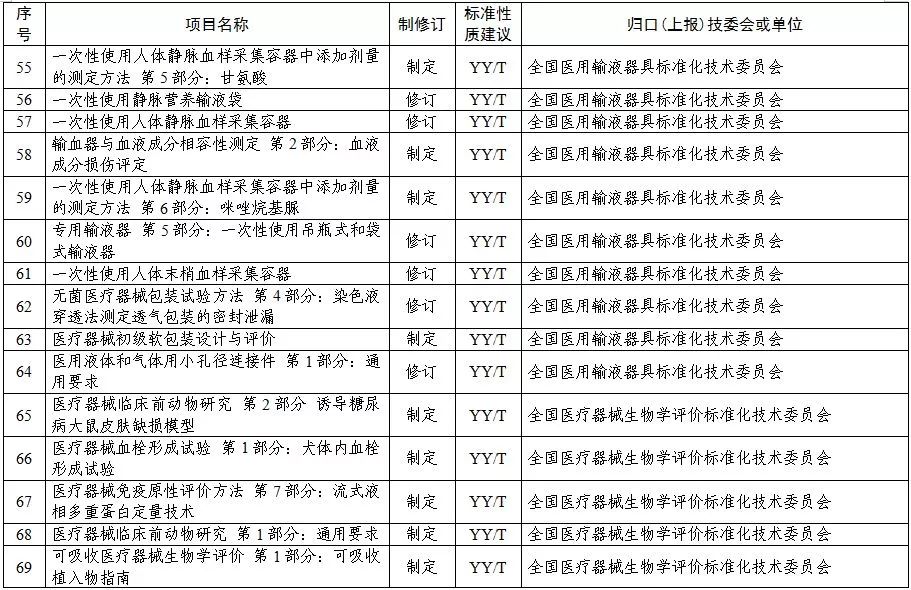
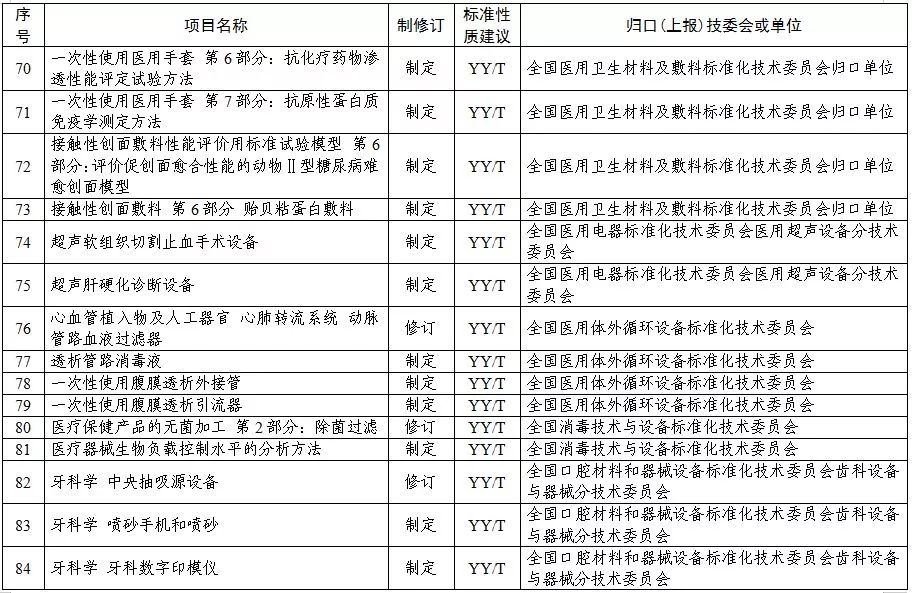
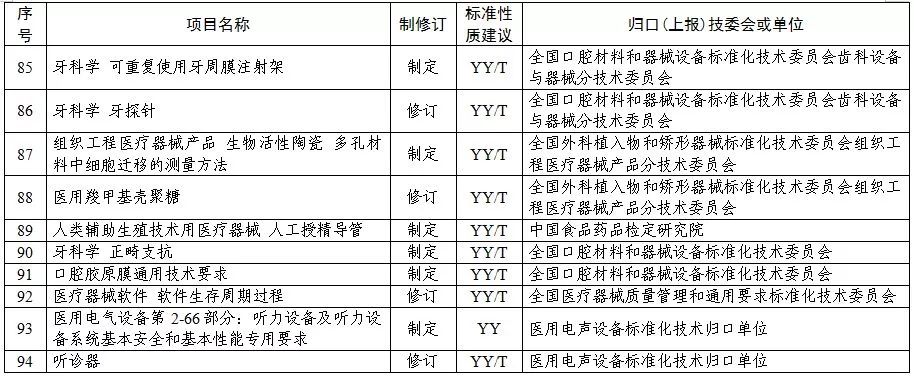
本文封面图片来源于图虫创意
[声明]本文来源于互联网转载,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性、准确性等负责,尤其不对文中产品有关功能性、效果等提供担保。本站文章版权归原作者所有,内容为作者个人观点,本站提醒读者,文章仅供学习参考,不构成任何投资及应用建议,如需转载,请联系原作者。如涉及作品内容、版权和其它问题,请与我们联系,我们将在第一时间处理!本站拥有对此声明的最终解释权。

